Trans-AT 聚酮合成酶(PKSs)是一類能夠合成大量結(jié)構(gòu)特殊���、活性多樣的聚酮分子的酶�����。這些酶中同時存在多種特殊模塊或結(jié)構(gòu)域�,如β-分支模塊�����、分支結(jié)構(gòu)域和BV氧化結(jié)構(gòu)域等�����,可在裝配線上直接對延伸的聚酮骨架進行修飾�,增加產(chǎn)物的結(jié)構(gòu)多樣性。然而����,在trans-AT PKS的非經(jīng)典催化過程中���,單一模塊或功能域的迭代使用過程尤為特殊。Lankacidin類天然產(chǎn)物是含大環(huán)內(nèi)酯結(jié)構(gòu)的聚酮肽雜合類天然產(chǎn)物���,具有抗菌�����、抗腫瘤等活性��,同樣是由trans-AT PKS合成����。前人研究發(fā)現(xiàn)�����,在lankacidin類天然產(chǎn)物的生物合成過程中���,四個trans-AT聚酮合酶模塊卻負責八輪聚酮骨架的延伸�,因此學術(shù)界長久以來認為該trans-AT PKS進行了未知的迭代作用�,但一直沒有找到證據(jù)。
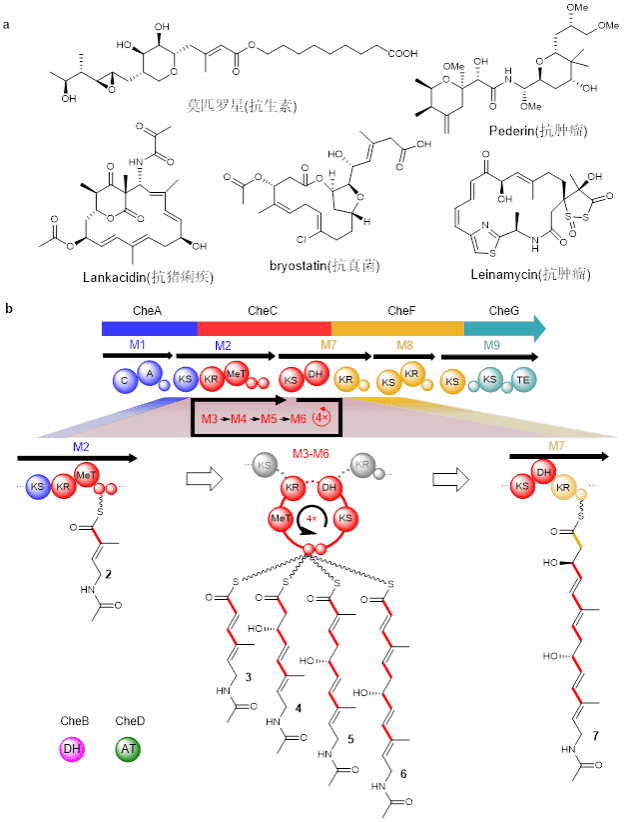
圖a��、優(yōu)良活性的trans-AT聚酮分子;b��、trans-AT聚酮合酶CheC的特殊迭代作用方式
為解決這一謎題�,該研究團隊通過蛋白質(zhì)異源表達和體外生化反應����,成功重建了整個trans-AT聚酮合酶生物合成途徑,搭建了體外生成系統(tǒng)��。通過化學合成潛在中間體���、體外重構(gòu)和捕獲生物合成中間體��,闡明了trans-AT聚酮合成酶在lankacidin類天然產(chǎn)物生物合成中的特殊迭代作用���。此外,還對trans-AT PKS中跨模塊作用的MT結(jié)構(gòu)域���、冗余的KS-ACP結(jié)構(gòu)域等進行了功能表征���。以經(jīng)典I型聚酮的“模塊化思維”對trans-AT聚酮合酶進行拆分和重構(gòu),并體外對新產(chǎn)生的模塊化trans-AT PKS進行功能驗證�����。將全部trans-AT聚酮合酶進行融合,產(chǎn)生出~763 KDa的重組酶并在大腸桿菌中實現(xiàn)了相應天然產(chǎn)物的生產(chǎn)�����,為trans-AT PKS的特殊迭代作用過程提供了直接實驗證據(jù)����。進一步研究表明,CheC酶具有獨特的KR–MT–ACP–ACP–KS–DH結(jié)構(gòu)域�����,這一結(jié)構(gòu)不僅能夠與前后的trans-AT聚酮合酶線性協(xié)作����,構(gòu)成完全功能的模塊,而且還能通過潛在的環(huán)形結(jié)構(gòu)自行組裝成一個非常規(guī)模塊���,促進生物合成過程中多輪聚酮延伸����。該研究挑戰(zhàn)了傳統(tǒng)的線性聚酮合酶的合成機制,揭示了trans-AT聚酮合酶在生物合成中的新功能�����,為未來trans-AT聚酮合酶的合理設計和工程化改造提供了新的思路����,也為聚酮肽雜合類天然產(chǎn)物的新藥研發(fā)提供充足原料。
南京大學生命科學學院麥振鵬博士為論文第一作者��,戈惠明教授���、譚仁祥教授和張博副教授為共同通訊,研究成果以“Lankacidin天然產(chǎn)物生物合成中trans-AT聚酮合酶的獨特作用機制研究(Insight into the role of a trans-AT polyketide synthase in the biosynthesis of lankacidin-type natural products)”為題�����,近期正式發(fā)表于國際學術(shù)期刊《自然?合成》(Nature Synthesis)雜志�����。論文鏈接:https://www.nature.com/articles/s44160-024-00599-1���。研究得到了基金委�����、科技部等的資助���。