肝細(xì)胞癌(Hepatocellular Carcinoma, HCC)是全球范圍內(nèi)最常見的惡性腫瘤之一,占所有肝癌病例的90%以上���。HCC 的早期癥狀不明顯����,大多數(shù)患者在確診時已處于疾病晚期����,治療選擇有限���,預(yù)后較差。目前����,HCC 的主要治療方法包括手術(shù)切除、肝移植�����、局部消融和系統(tǒng)治療等����。然而���,由于 HCC 的高度異質(zhì)性和復(fù)雜的生物學(xué)行為���,這些治療方法的療效往往不盡如人意。近年來����,免疫治療在 HCC 的治療中取得了顯著進(jìn)展���,尤其是免疫檢查點(diǎn)抑制劑的應(yīng)用,為 HCC 患者帶來了新的希望�。然而,盡管免疫檢查點(diǎn)抑制劑(如抗PD-1療法)和靶向藥物在晚期HCC治療中取得進(jìn)展�����,但患者響應(yīng)率差異顯著���,亟需探索新的治療靶點(diǎn)以改善療效�����。
近年來��,蛋白質(zhì)翻譯后修飾(PTM)在腫瘤發(fā)生中的作用備受關(guān)注��,其中SUMO化(SUMOylation)作為一種可逆的修飾過程��,通過調(diào)控蛋白穩(wěn)定性�、互作能力及亞細(xì)胞定位參與癌癥進(jìn)展����。SUMO特異性蛋白酶家族(SENPs)負(fù)責(zé)去SUMO化修飾�,SENP3 是 SUMO 特異性肽酶家族的一員�,能夠去除蛋白質(zhì)上的 SUMO 修飾,從而調(diào)節(jié)蛋白質(zhì)的功能���。SENP3 在多種癌癥中表達(dá)異常����,包括肝細(xì)胞癌���、乳腺癌�、前列腺癌和結(jié)直腸癌等�����。然而�����,SENP3 在 HCC 中的具體作用及其分子機(jī)制尚不完全清楚���。
在最新的研究中,南京大學(xué)醫(yī)學(xué)院江春平/吳俊華團(tuán)隊(duì)發(fā)現(xiàn),SENP3在HCC中顯著高表達(dá)�,并通過調(diào)控腫瘤細(xì)胞內(nèi)在惡性表型和重塑免疫微環(huán)境雙重機(jī)制促進(jìn)肝癌進(jìn)展。更關(guān)鍵的是�����,靶向抑制SENP3不僅抑制腫瘤生長�����,還可顯著增強(qiáng)抗PD-1療法的效果�����,該研究為HCC治療提供了全新策略�����。
這項(xiàng)研究首先通過Kaplan-Meier 生存分析及TCGA 和 ICGC 數(shù)據(jù)庫的分析發(fā)現(xiàn) SENP3 在 HCC 組織中的表達(dá)水平顯著高于正常肝組織��,緊接著研究團(tuán)隊(duì)通過 qPCR ���, Western blot 以及免疫組化(IHC)實(shí)驗(yàn)對臨床樣本進(jìn)行分析證實(shí)�,SENP3在HCC組織中顯著高表達(dá)���,且與患者預(yù)后不良密切相關(guān)�����,這都揭示了SENP3在HCC惡性進(jìn)展中發(fā)揮重要作用(圖1)�。
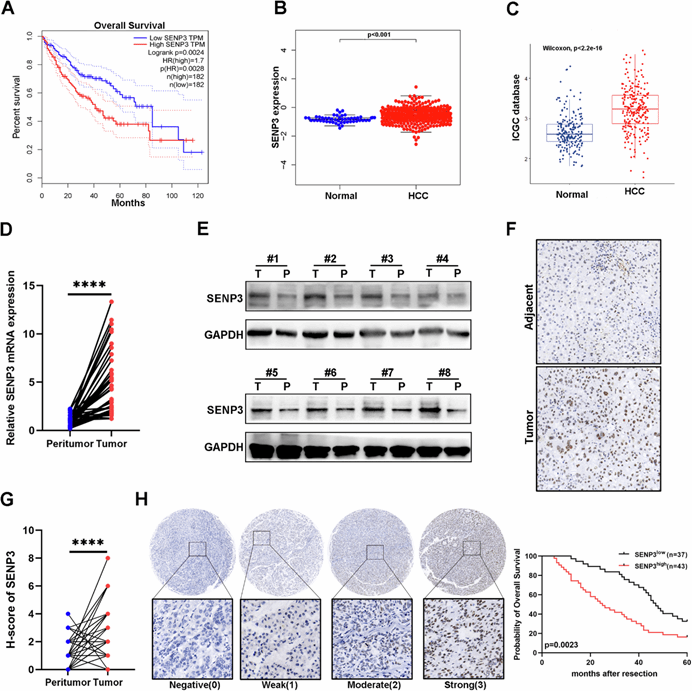
圖1. SENP3 在 HCC 組織中高表達(dá)并與患者生存率負(fù)相關(guān)
研究團(tuán)隊(duì)對SENP3 在 HCC 中的具體作用進(jìn)行深入的探究。首先通過多種體外功能實(shí)驗(yàn)揭示了敲低SENP3可抑制肝癌細(xì)胞的增殖����、遷移和侵襲能力,并促進(jìn)肝癌細(xì)胞凋亡���;而過表達(dá)SENP3則加劇惡性表型(圖2)��。隨后����,在多種小鼠模型(皮下移植瘤��、肺轉(zhuǎn)移模型和原位肝腫瘤模型)中對SENP3的具體作用進(jìn)行體內(nèi)實(shí)驗(yàn)驗(yàn)證��,結(jié)果顯示SENP3的缺失顯著抑制腫瘤生長和轉(zhuǎn)移(圖3)��。體內(nèi)和體外實(shí)驗(yàn)共同證明了SENP3是HCC惡性進(jìn)展的關(guān)鍵驅(qū)動因子及其是腫瘤生長和轉(zhuǎn)移中的關(guān)鍵因子����。
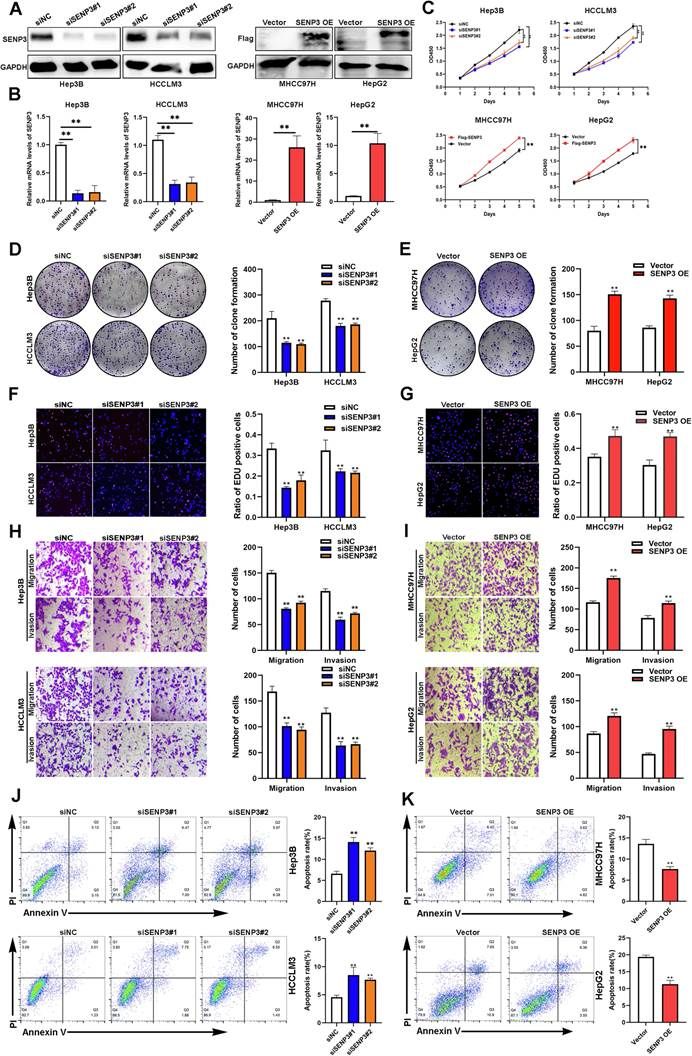
圖2. SENP3 在體外促進(jìn) HCC 細(xì)胞惡性表型的形成
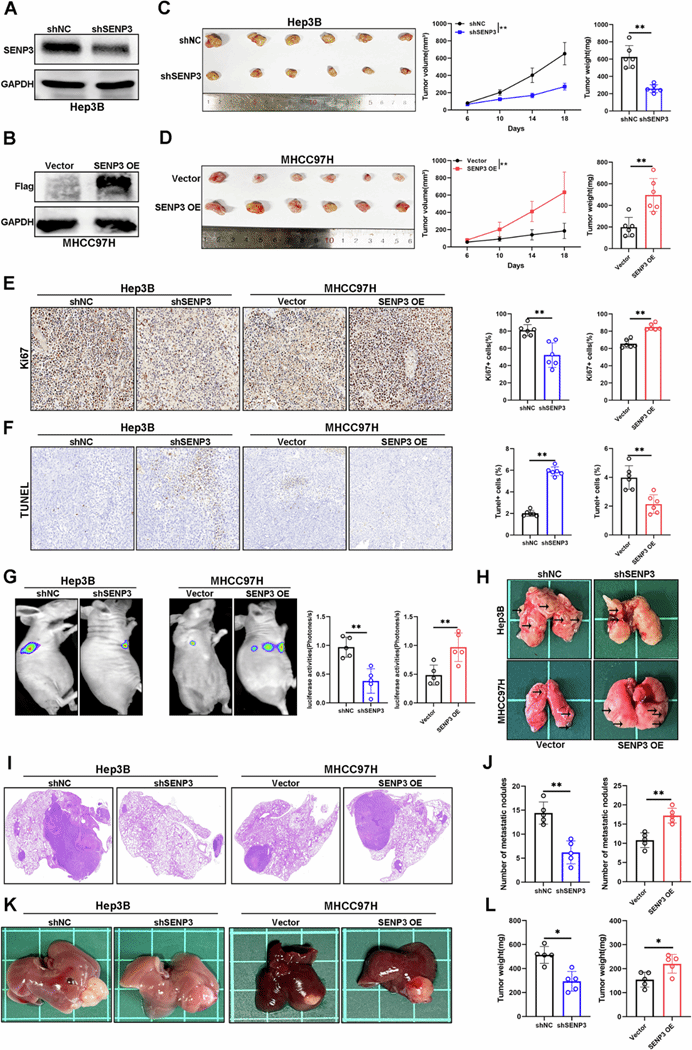
圖3. SENP3 在體內(nèi)促進(jìn) HCC 的生長和轉(zhuǎn)移
研究團(tuán)隊(duì)緊接著對SENP3在HCC中的具體作用機(jī)制展開了研究,通過一系列實(shí)驗(yàn)�,研究團(tuán)隊(duì)發(fā)現(xiàn)SENP3能夠直接與RACK1結(jié)合,并且能夠去除RACK1上的SUMO2/3修飾��,特別是RACK1的K264和K271位點(diǎn)�����。這一去SUMO化作用增加了RACK1的穩(wěn)定性�����,并促進(jìn)了RACK1與PKCβII的相互作用�,從而影響下游信號通路的激活(圖4)。團(tuán)隊(duì)進(jìn)一步探討了SENP3對RACK1穩(wěn)定性和功能的影響���。實(shí)驗(yàn)結(jié)果顯示����,SENP3的表達(dá)水平能夠調(diào)節(jié)RACK1的蛋白穩(wěn)定性��,敲低SENP3會導(dǎo)致RACK1的泛素化增加�,從而加速其降解����,而SENP3過表達(dá)則相反�。此外,SENP3通過去SUMO化修飾RACK1����,增強(qiáng)了RACK1與PKCβII的結(jié)合,從而促進(jìn)了eIF4E的磷酸化和相關(guān)癌基因的翻譯�,進(jìn)一步推動了HCC細(xì)胞的惡性表型(圖5)。此外�,SENP3-RACK1軸還通過調(diào)控核糖體功能增強(qiáng)腫瘤細(xì)胞的代謝適應(yīng)性。
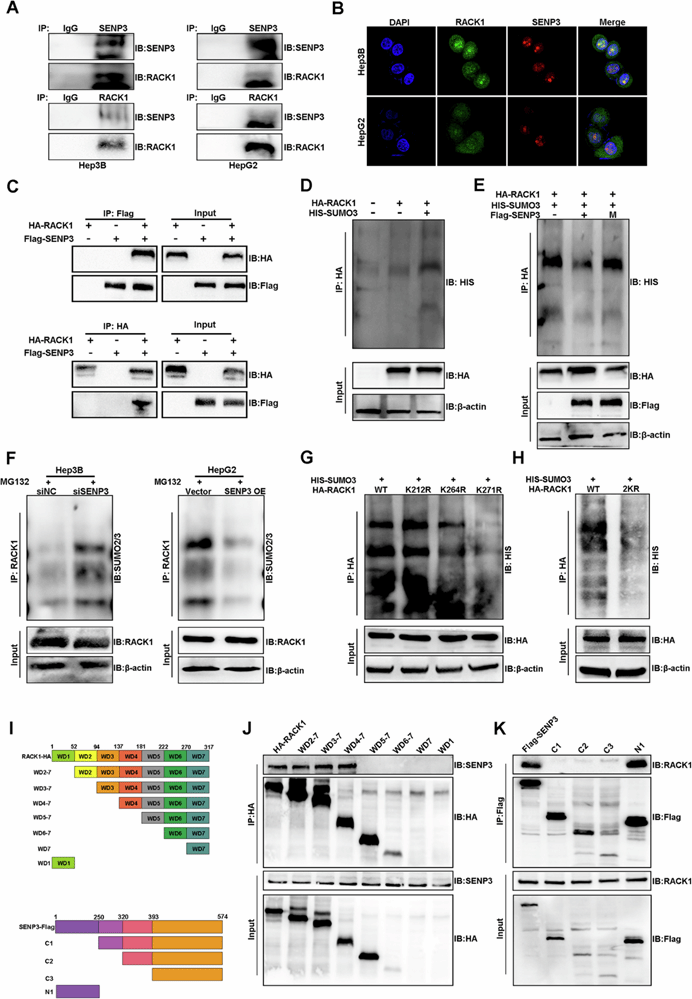
圖4. SENP3解除了SUMO2/3對RACK1的控制
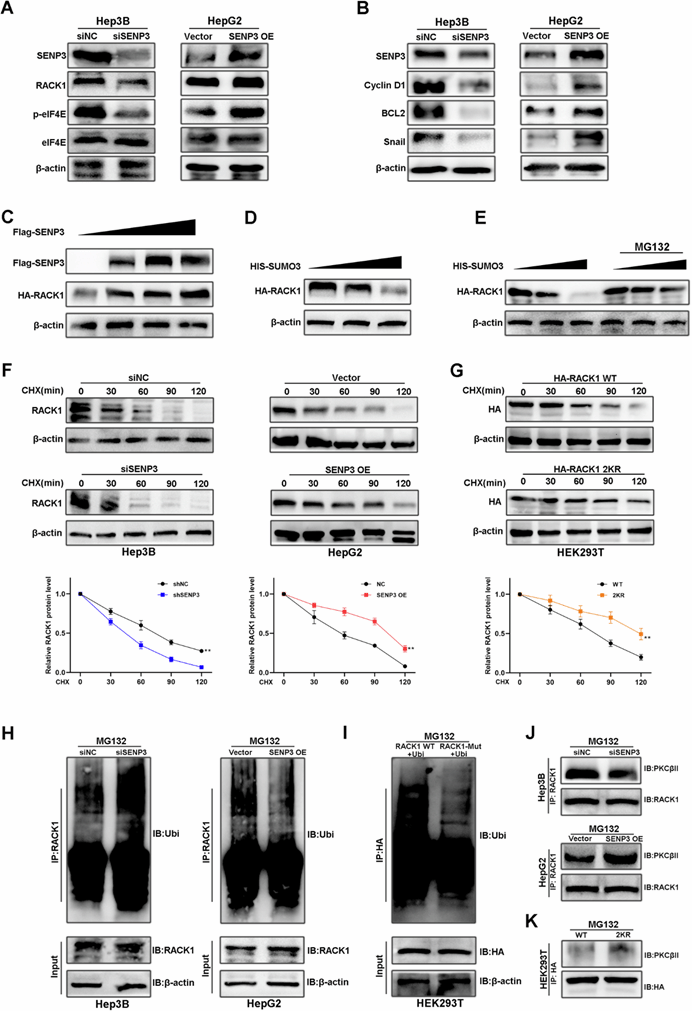
圖5. SENP3 可促進(jìn) RACK1 的穩(wěn)定性及其與 PKCβII 的相互作用
團(tuán)隊(duì)進(jìn)一步研究發(fā)現(xiàn)��,腫瘤內(nèi)源性SENP3通過促進(jìn)腫瘤相關(guān)巨噬細(xì)胞(TAMs)的浸潤來重塑免疫微環(huán)境�,從而抑制抗腫瘤免疫反應(yīng)。在免疫健全小鼠中�����,SENP3敲低顯著抑制了腫瘤生長并延長了總體生存時間����,而在免疫缺陷小鼠中上述效果較弱�����。流式細(xì)胞術(shù)分析顯示,SENP3敲低減少了TAMs的浸潤���,同時增加了CD8+ T細(xì)胞和NK細(xì)胞的數(shù)量�,而SENP3過表達(dá)則相反�����。此外����,巨噬細(xì)胞的缺失可以逆轉(zhuǎn)SENP3介導(dǎo)的腫瘤促進(jìn)作用,進(jìn)一步證實(shí)了SENP3通過招募TAMs來促進(jìn)腫瘤生長(圖6)����。同時,研究團(tuán)隊(duì)也揭示了SENP3通過上調(diào)CCL20的表達(dá)來促進(jìn)TAMs的招募��,從而重塑免疫微環(huán)境���。在實(shí)驗(yàn)中���,SENP3敲低顯著降低了CCL20的蛋白水平�����,而SENP3過表達(dá)則顯著增加了CCL20的蛋白水平�����。此外��,SENP3主要通過調(diào)節(jié)CCL20的翻譯效率來影響其蛋白水平����,而不是通過mRNA水平����。過表達(dá)RACK1可以部分恢復(fù)SENP3敲低對CCL20分泌的影響,這表明SENP3通過RACK1依賴的方式調(diào)節(jié)CCL20的翻譯過程(圖7)����。
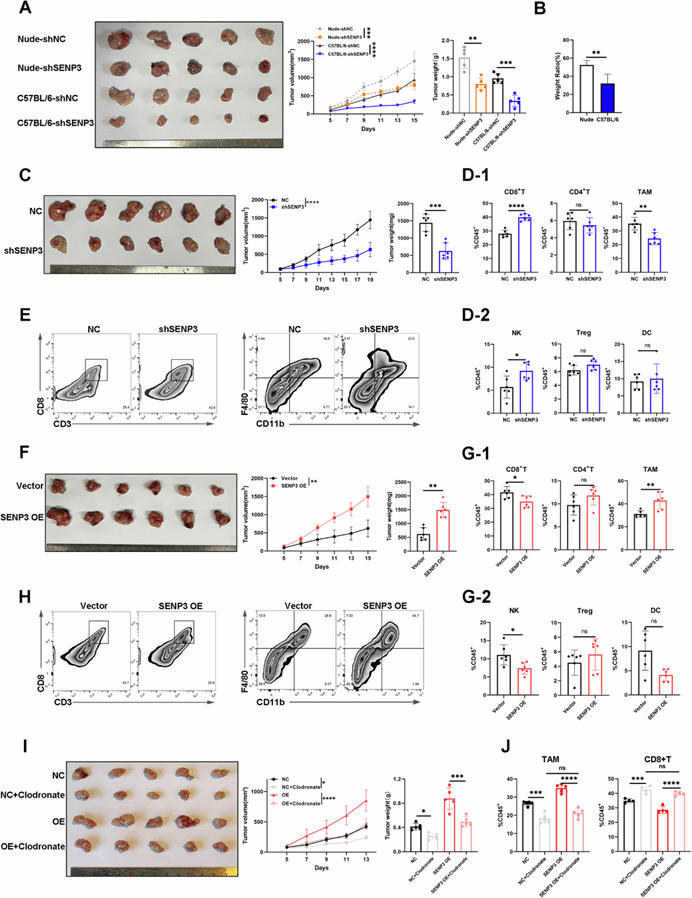
圖6. 腫瘤內(nèi)源性 SENP3 通過促進(jìn) HCC 中腫瘤相關(guān)巨噬細(xì)胞的浸潤來重塑免疫微環(huán)境
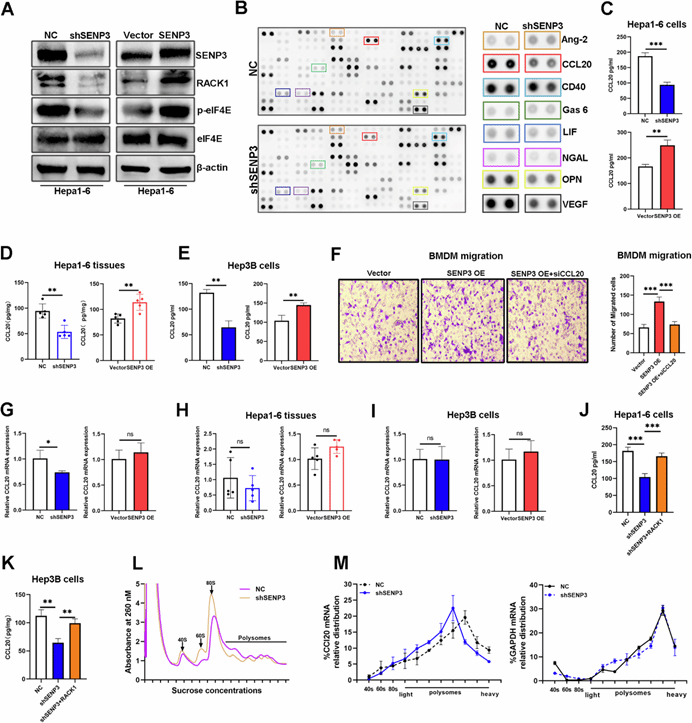
圖7. SENP3 通過上調(diào) CCL20 表達(dá)促進(jìn)腫瘤相關(guān)巨噬細(xì)胞的募集
最后,研究團(tuán)隊(duì)發(fā)現(xiàn)在化學(xué)誘導(dǎo)的HCC模型中�����,肝特異性敲低SENP3顯著減少腫瘤數(shù)量和體積����。聯(lián)合使用SENP3抑制劑與抗PD-1抗體可顯著增強(qiáng)療效,相較于單一治療組�,聯(lián)合治療組腫瘤體積縮小超過60%。這一協(xié)同效應(yīng)歸因于SENP3抑制后TAMs減少和CD8+ T細(xì)胞活性增強(qiáng)����,從而重塑腫瘤免疫微環(huán)境(圖8)。
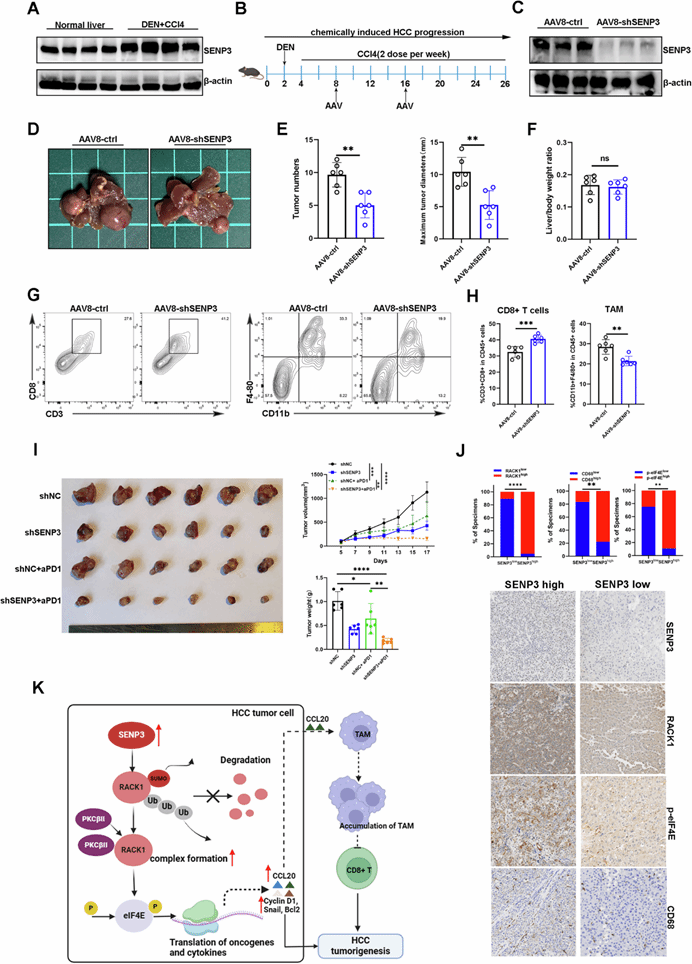
圖8. 靶向 SENP3 抑制 HCC 的進(jìn)展并增強(qiáng)抗 PD-1 治療的療效
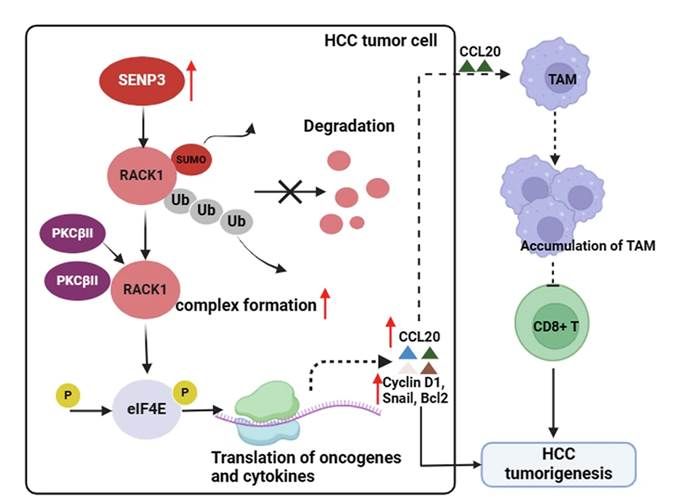
圖8K. 本研究的主要發(fā)現(xiàn)與模式機(jī)制圖���,揭示了SENP3/RACK1軸驅(qū)動HCC進(jìn)展與免疫逃逸的機(jī)制
本研究首次揭示了SENP3在HCC中的雙重作用機(jī)制����,發(fā)現(xiàn) SENP3 通過促進(jìn)腫瘤相關(guān)巨噬細(xì)胞(TAMs)的浸潤和重塑免疫微環(huán)境�����,增加腫瘤微環(huán)境(TME)中調(diào)節(jié)性 T 細(xì)胞(Treg)的浸潤�����,從而抑制抗腫瘤免疫反應(yīng)�����。該研究不僅闡明了SUMO化修飾在HCC中的新機(jī)制,還創(chuàng)新性地將腫瘤細(xì)胞內(nèi)在信號與免疫微環(huán)境調(diào)控相結(jié)合�,為聯(lián)合治療提供了重要靶點(diǎn)。
近日�,南京大學(xué)醫(yī)學(xué)院江春平教授/吳俊華教授團(tuán)隊(duì)在Cell Death & Differentiation上發(fā)表了題為“SENP3 inhibition suppresses hepatocellular carcinoma progression and improves the efficacy of anti-PD-1 immunotherapy”的研究論文。南京大學(xué)醫(yī)學(xué)院博士生汪鵬和博士畢業(yè)生仇建南等人為該研究論文的共同第一作者��。南京大學(xué)醫(yī)學(xué)院江春平教授����、吳俊華教授和王忠夏副主任醫(yī)師等人為該論文的共同通訊作者。該研究得到了國家自然科學(xué)基金(82772819����、81972888)、省實(shí)驗(yàn)室項(xiàng)目(編號SY5202202����、JNL-202219B、JNL-202204A以及JNL-2023017D)及省重點(diǎn)研發(fā)計劃(BE2022840)的資助�。
原文鏈接:https://doi.org/10.1038/s41418-024-01437-9